Sterilisera insekter med strålning
Sedan 1950-talet har olika arter av insekter steriliserats med hjälp av strålning och sedan släppts ut i sin naturliga miljö. Det är ett sätt att minska en population av insekter som sprider sjukdomar, eller insekter som skadar det vi odlar. Logiken bakom det är att när sterila hanar parar sig med honor i naturen produceras ingen avkomma och populationen minskar. Det har fungerat väl i många fall. I USA har man till exempel lyckats utrota Cochliomyia hominivorax, en typ av spyfluga vars larver lever av kött från varmblodiga djur.
En nackdel med tekniken är att insekternas överlevnadsförmåga kan försämras på grund av strålningen. Det gör att de sterila insekterna får svårare att konkurrera med sina artfränder i naturen. En annan nackdel är att steriliseringen inte alltid fungerar till 100 procent och att det är svårt att separera hanar från honor. Bäst fungerar nämligen strategin om det är sterila hanar som släpps ut. När insekter steriliseras med hjälp av strålning är de inte genetiskt modifierad.
Modifiera myggor för sjukdomsbekämpning
Malaria orsakas av encelliga parasiter som tillhör släktet Plasmodium och sprids via Anopheles-myggor. När en honmygga biter en infekterad människa får hon med sig både blod och sporozoiter, ett tidigt stadium av parasiten. Den färdigutvecklade parasiten tar sig till myggans spottkörtlar och infekterar nästa person myggan biter. Denguefeber, zika, gula febern och chikungunyafeber orsakas av virus och sprids från människa till människa via myggor av släktet Aedes. På flera håll i världen pågår forskning och utveckling där målet är att med hjälp av genteknik minska sjukdomsspridningen.
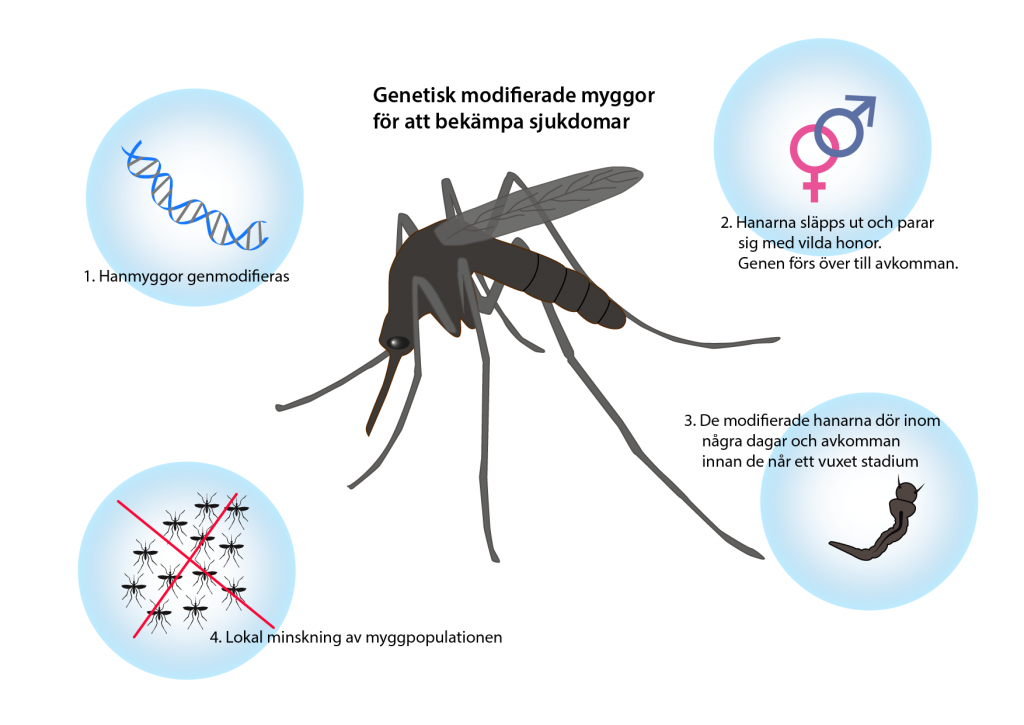
Det brittiska företaget Oxitec har genetiskt modifierat myggarten Aedes aegypti och två arter av malariamyggor, Anopheles albimanus och Anopheles stephensi. Det är bara hanar som modifieras och när de släpps ut parar de sig med vilda honor. Den gen som hanarna modifierats med producerar ett protein som gör att avkomman inte överlever till ett vuxet stadium. Det gör i sin tur att insektspopulationen minskar lokalt. De modifierade hanarna bär också på en gen för ett protein som under ett visst ljusspektrum lyser upp insektskroppen. Det gör det enklare att följa insekterna när de släpps ut i miljön. Metoden har testats på flera håll i världen, både i nätburar och i insekternas naturliga miljö. Miljontals modifierade Aedes-myggor har till exempel släppt ut i olika delar av Brasilien med goda resultat.
Det icke-vinstdrivande forskningskonsortiet Target Malaria har som mål att utveckla och dela med sig av tekniker för att kontrollera malaria i Afrika söder om Sahara. Forskarna inom projektet arbetar i Burkina Faso, Mali, Uganda och Ghana och har genetiskt modifierat hanmyggor så att de blir sterila. När de släpps ut och parar sig med honor i naturen får de därför ingen avkomma. De modifierade myggorna har hittills testats i sin naturliga miljö i Burkina faso. Försöket startade 2019 och var småskaligt. Mindre än 10 000 modifierade malariamyggor av arten Anopheles gambiae släpptes ut.
Skydda odlingar med modifierade skadegörare
Skadegörare på citrusfrukter, melon och persika
Borrflugan Ceratitis capitata är en skadegörare på mer än 250 växtarter. Den angriper bland annat citrusfrukter, melon och persika. Flugan hör ursprungligen hemma i Afrika kring ekvatorn, men har spridit sig så att den nu även finns i till exempel Australien, Latinamerika och i medelhavsområdet. Borrflugan lägger sina ägg i frukten och när larverna utvecklas äter de av fruktköttet och skapar tunnlar där bakterier och svampar kan få fäste.

Hanar av borrflugan har genetiskt modifierats på så sätt att avkommor som är honor inte överlever. De modifierade flugorna har ännu inte testats i sin naturliga miljö, men under mer kontrollerade förhållanden i Storbritannien, Grekland, Brasilien, Marocko och Australien.
Skadegörare på kål
Kålmalens larver är en skadegörare på kålväxter som raps, vitkål och broccoli. Globalt orsakar larven förluster på i storleksordningen 4–5 miljarder amerikanska dollar per år. Kålmalen är resistent mot de flesta växtskyddsmedel, både kemiska och biologiska. Hanar av kålmalen har genetiskt modifierats så att honorna i avkomman inte överlever. Eftersom det är honorna som lägger ägg som utvecklas till larver som äter av grödan, så minskar skadorna. De modifierade kålmalarna har ännu så länge bara testats i liten skala
Sterilisera insekter med gensax
Som ett alternativ till strålning har forskare testat att använda gensaxen CRISPR/Cas9 och slagit ut gener i bananflugans genom. Det ledde till att inga honor utvecklades och att 100 procent av hanarna blev sterila. Att man använde bananfluga beror på att de är en modellorganism, men de gener som slogs ut i bananflugans arvsmassa är vanliga även i andra insektsarter. Det innebär att tekniken troligtvis även skulle kunna användas på till exempel myggor som sprider sjukdomar och på växtskadegörare.
Uppdaterad november 2020.

